La carte des isotopes
La carte des isotopes
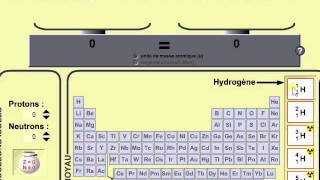
Conséquence immédiate de la découverte du neutron, tout noyau peut désormais être défini par deux entiers, son nombre de protons (Z), et son nombre de neutrons (N). La masse atomique (A) n’est ni plus ni moins que la somme (N + Z). Partant de là, on va savoir classer tous les noyaux existants, et même prévoir la place de ceux que l’on n’a pas encore découverts. Il suffit de dresser un tableau rectangulaire, dans lequel on reporte N selon la dimension horizontale, par exemple, et Z selon la dimension verticale. Chaque case correspond à un couple de valeurs (N,Z), donc à un noyau donné.
Bien entendu, tous les noyaux connus viennent se ranger docilement dans ce tableau, appelé carte des noyaux, ou carte des isotopes dont le début est représenté sur la figure 32. Mais, nous sommes en 1932, et, par rapport à ce que nous connaissons aujourd’hui, cette carte est presque vide. Elle ne comprend que des noyaux naturels, dont la grande majorité est stable. Ceux-ci se regroupent autour d’une ligne orientée du sud-ouest au nord-ouest (en utilisant le langage habituel des cartes), connue sous le nom de « ligne de stabilité » des noyaux. Cependant, dans la région des noyaux légers, la carte ne tardera pas à se garnir et dans celle qui concerne les noyaux les plus lourds, on trouve déjà, bien entendu, tous les isotopes radioactifs des familles naturelles.
Vidéo : La carte des isotopes
Vidéo démonstrative pour tout savoir sur : La carte des isotopes
2 réponses pour "La carte des isotopes"
la carte des isotopes
pourquo Lhomme a la peau blanche a toujour plus davance sur les hommes noire?